发布时间:2019-01-29
目前有超过15000种药物被美国FDA批准,而药物靶点至少有800个。对某些药物而言,是没有明确的靶点(如某些麻醉剂与利尿药)的,而只有10-15%的人类疾病蛋白质靶标可以找到小分子药物。因此药物作用新靶标的数量是非常有限。据估计,在人体内大约有85-90%的“不可成药(undruggable)”靶标,有70%的激酶家族是不可成药靶标;最大的可成药靶点(drug-targeted)蛋白家族是G蛋白受体(GPCRs),但也只有79个是可成药靶点,至少有58%的GPCRs处于未开发状态或非成药状态。所以说,药物开发仍有很大的研究空间,尤其是研究“非成药靶点”,可能使药物发展至新的高度。今天所说的磷酸酶就是众多靶点中的代表。
非成药靶点中研究较为广泛的几类靶点一览表
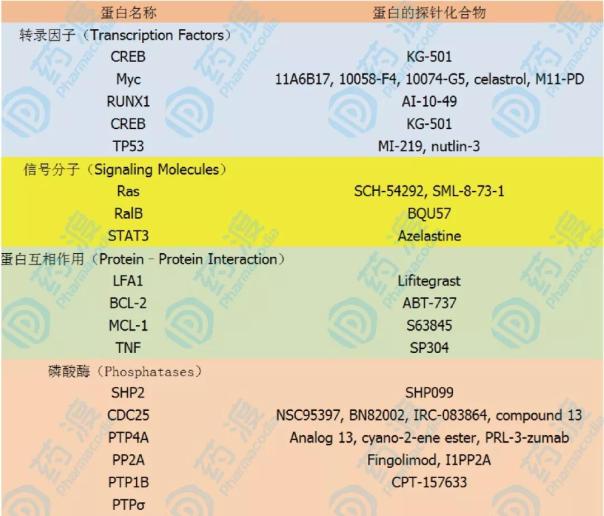
1、为什么选择开发磷酸酶抑制剂?
磷酸酶(phosphatase)对许多生物学功能至关重要,因为磷酸化(通过蛋白激酶)和去磷酸化(通过磷酸酶)在细胞调节和信号传导中起着至关重要作用,与肥胖、糖尿病、癌症、神经退行性等疾病有着千丝万缕的联系。虽然目前已有很多安全有效的以磷酸激酶作为靶点的药物上市,但是靶向磷酸酶的药物却是难以寻觅。
临床前与进行临床试验的药物。
目前进入临床的磷酸酶抑制剂包括Novartis的SHP2 抑制剂TNO155、Sanofi 的SHP2抑制剂TNO155及InFlectis BioScience的 PPP1R15A 抑制剂IFB-088等药物,还有多种临床前药物。这些磷酸酶抑制剂均有活性的结合位点,但是它们却是更多地与结合“口袋”之外的变构位点结合。基于这些现象,变构药物的研究可能将是磷酸酶抑制剂研发成功的关键所在。并且一些创新药物公司已经注意到这个问题,他们专注于研究变构药物的研发,并不断改善候选化合物的活性。
蛋白酪氨酸磷酸酶1B(PTP1B)是PTP(protein tyrosine phosphatase,蛋白酪氨酸磷酸酶)蛋白家族一员,由冷泉实验室的Nick Tonks于1980年代末发现,至1990年代末,已有动物模型表明PTP1B是胰岛素信号通路的重要节点,使胰岛素受体去磷酸化并失活,进而使人体出现糖尿病与肥胖。研究发现该蛋白也与免疫作用相关,抑制PTP1B,可以降低实验动物的死亡率;还有研究显示PTP1B 与PTK HER2基因在乳腺癌细胞中共同过量表达。所以PTP1B是一个很有前途的靶点,PTP1B抑制剂是治疗Ⅱ型糖尿病、肥胖、免疫缺陷及乳腺癌的潜在药物,但是从发现至今将近30年时间没有一款药物上市。
DPM-1001是目前进入临床前的一种高效及特异性的PTP1B抑制剂,由DepYmed公司研发。该药为口服制剂,不仅用于治疗糖尿病及肥胖,还用于治疗HER2+ 乳腺癌及Wilson病。

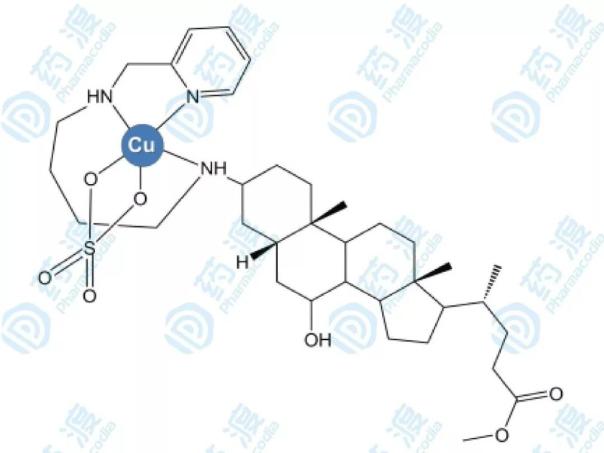
DPM-1001的化学结构式
实验证明,DPM-1001是一种高效的非竞争性抑制剂,其IC50值为10nM。理论上PTP家族蛋白作为带电荷的底物,往往是带电荷的抑制剂才可以很好地进入到PTP1B的活性口袋中。通常来说,这类化合物不适合口服给药,因生物利用度差并且难以穿过细胞膜。但是DPM-1001解决了这些问题,它不仅可以口服给药,并且十分的高效。DPM-1001与PTP1B的C末端结合,组成稳定的Cu-DPM-1001复合物,这是其高效性的重要解释。DPM-1001抑制PTP1B后,增强胰岛素通路的信号转导,降低血糖浓度,有效抑制因饮食导致的肥胖问题。而对于乳腺癌来说,应用DPM-1001之后,减缓了肿瘤的生长速度并降低了癌症向肺部转移的可能性。
DPM-1001与Cu2+发生络合反应
药物AKB-9778作用于靶点VE-PTP(血管内皮细胞蛋白酪氨酸磷酸酶,vascular endothelial-protein tyrosine phosphatase),由Aerpio Pharmaceuticals公司研发。VE-PTP可以调节TIE2的活性,上调缺氧内皮细胞,使血管发生病变。AKB-9778作为小分子抑制剂,抑制VE-PTP的活性,激活TIE2,是一种高效特异性VE-PTP的抑制剂,对于VE-PTP,其IC50为17pM,而对于PTPIB的IC50为780 nM,说明其对VE-PTP具有高度特异性。大量实验表明,AKB-9778对视网膜内皮细胞的TIE2有上调作用,抑制视网膜和脉络膜新生血管的生成。此外,AKB-9778还可以阻断VEGF(血管内皮生长因子)与组胺介导的血管渗漏,还有抑制肿瘤血管生成的作用。
近期临床试验显示,AKB-9778对糖尿病肾病与糖尿病视网膜病变有治疗作用,联合VEGF抑制剂对糖尿病视网膜病变有更好的效果。AKB-9778是皮下注射给药,药物动力学研究表明AKB-9778很快进入循环并迅速到达靶组织——视网膜脉管系统。目前,该药已进入临床试验IIb期。

PTP抑制剂也不乏失败的例子,ertiprotafib是惠氏公司研发的PTP1B抑制剂,用于治疗2型糖尿病。该药对PTP1B的 IC50为1.6 μM,IKK-β的 IC50为400nM,对PPARα与PPARβ的EC50约为1μM,说明该药靶向性不高,并且还对其他靶点产生影响,从而产生诸多不良反应,使其于2002年停止在临床II试验中。虽然目前的两款PTP抑制剂有较高的靶向性,但由于临床试验漫长,药物治疗效果仍需长期监测,PTP抑制剂上市之路仍任重道远。
磷酸酶(phosphatase)对许多生物学功能至关重要,因为磷酸化(通过蛋白激酶)和去磷酸化(通过磷酸酶)在细胞调节和信号传导中起着至关重要作用,与肥胖、糖尿病、癌症、神经退行性等疾病有着千丝万缕的联系。虽然目前已有很多安全有效的以磷酸激酶作为靶点的药物上市,但是靶向磷酸酶的药物却是难以寻觅。
临床前与进行临床试验的药物
目前进入临床的磷酸酶抑制剂包括Novartis的SHP2 抑制剂TNO155、Sanofi 的SHP2抑制剂TNO155及InFlectis BioScience的 PPP1R15A 抑制剂IFB-088等药物,还有多种临床前药物。这些磷酸酶抑制剂均有活性的结合位点,但是它们却是更多地与结合“口袋”之外的变构位点结合。基于这些现象,变构药物的研究可能将是磷酸酶抑制剂研发成功的关键所在。并且一些创新药物公司已经注意到这个问题,他们专注于研究变构药物的研发,并不断改善候选化合物的活性。本文接上篇《磷酸酶是不能成药靶点?总有人不信邪...(一)》。
SHP2也属于PTP蛋白家族,与乳腺癌、肺癌等多种癌症的发生密切相关,此外,SHP2还调节PD-1介导的信号转导,并参与免疫检查点通路的调节。最近,有研究称,SHP2可以增强RAS/MAP通路,从而促进肿瘤细胞的生长。这个发现具有重要意义,因为RAS/MAP通路是最重要的癌症通路之一,抑制RAS/MAP信号通路,可能会给多种癌症治疗带来新的机遇。
TNO155是由Novartis公司研发的SHP2抑制剂,是由先导化合物SHP099发展而来,已进入临床试验I期。口服给药后, TNO155抑制MAPK的信号转导,并减少了SHP2的过量表达,进而减缓肿瘤细胞的生长。目前TNO155仍未被披露有效信息。但作为先导化合物SHP099却有着深入的研究。SHP099对SHP2的IC50为0.071μM,是一个活性较强的化合物,但它对SHP1无活性,同时它也是一个安全性较高的药物,每天给予实验动物100mg/kg的药物即可达到抑制肿瘤生长的作用。

SHP099的化学结构式
另一种SHP2抑制剂RMC-4630由Revolution Medicines公司研发。Revolution Medicines作为创新型药物研发公司,致力于小分子磷酸酶抑制剂的开发。RMC-4630也是SHP099的类似物,对多种肿瘤,如非小细胞肺癌的生长具有抑制作用。目前该药的临床前研究已经完成,即将进入临床试验I期。同时,Revolution Medicines公司也开发了一种SHP1抑制剂。SHP1与SHP2的作用机制类似。该药目前处于临床前研究中,所披露资料较少。
针对SHP-1的抑制剂葡萄糖酸锑钠(sodium stibogluconate,SSG)也进入临床I期试验。SSG并非新药,最初作为治疗利什曼病的药物进入临床,但由于其严重的副作用而限制使用,直到有研究称其具有抗肿瘤活性。该药是否能够成功上市还有待观察。
PPP1R15A也是PTP家族的一员,而PPP1R15A的过量表达可能导致蛋白质的错误折叠,针对错误折叠蛋白质的异常积累,细胞会启动保护机制,使真核翻译启动因子2α(eIF2α)暂时性磷酸化,减少蛋白质错误折叠。有一种叫guanabenz的抗高血压药物可以延长eIF2α的磷酸化时间,并抑制PPP1R15A的信号传导。研究人员将该药物作为先导化合物研究,但是长时间追踪发现,guanabenz会导致小鼠神经系统紊乱,不良反应较大,于是被放弃了。之后Das等人合成guanabenz的衍生物sephin 1,发现它能够抑制PPP1R15A的信号转导,纠正这种蛋白质错误折叠。该药有良好的药物动力学参数,并且靶向中枢神经与外周神经系统。Sephin 1被授权给法国制药公司InFlectis BioScience,并改名为IFB-088,目前处于临床试验I期,用于治疗遗传性原发性运动感觉性神经病(Charcot-Marie-Tooth disease,CMT)的1A、1B亚型。
LB-100由Lixte Biotechnology公司研发,作用于磷酸酶2A(proteinphosphatase 2A,PP2A)。PP2A是丝氨酸/苏氨酸磷酸酶,参与了细胞代谢、DNA 复制、基因表达、信号转导、细胞分化及凋亡等多个过程。LB-100作为PP2A的抑制剂,具有增强免疫检查点抑制剂的抗肿瘤活性,对晚期肿瘤生长具有抑制作用,该药也可以用于治疗中风、2型糖尿病、心脏病及重度抑郁症。目前LB-100已经顺利完成临床I期试验,对多种实体瘤具有治疗作用,并且该药物的安全性高,耐受性好。
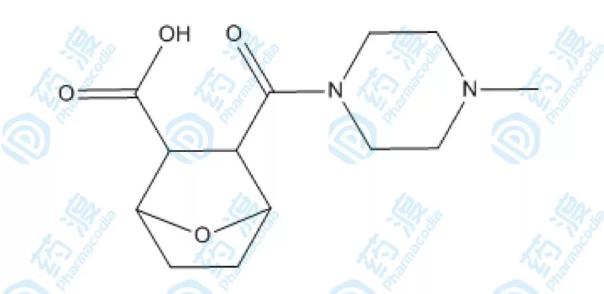
LB-100的化学结构式
PRL3-zumab是一款人源化单克隆抗体药物,作用于PRL-3( phosphatase of regenerating liver,肝再生磷酸酶-3)。PRL家族有三个成员,其中PRL-3与癌症转移有关。据以往调查,在多种转移性恶性肿瘤中,PRL-3都有极高的表达,而原发癌症与正常组织却没有表达。PRL3-zumab是由新加坡科技研究局(A*STAR)研发,通过高通量筛选得到,用于治疗胃癌。后发现在原发性胃癌中,约有70%患者会出现PRL-3过表达,这导致患者手术后较短的生存期。PRL3-zumab作为人源化单克隆抗体具有很强的优势,首先它不会发生免疫性反应,其次,与传统化疗药物相比,它有很强的专一性,减少副作用,增加药物安全性与患者耐受性。目前该药处于临床I期试验。
AQX-1125是惟一的SHIP-1(SH-2 containing inositol 5’polyphosphatase 1, 多磷酸肌醇-5-磷酸酶1)抑制剂,由Aquinox Pharmaceuticals公司研发。SHIP-1在肿瘤生长与免疫调节中也具有重要作用,SHIP-1参与PI3K/AKT信号通路的调节,这也是肿瘤的重要通路之一(该通路我也进行过讨论,有兴趣的请参考PI3K抑制剂——癌症患者的新选择这篇文章)。AQX-1125不仅具有抗肿瘤活性,且因对PI3K有抑制作用,因此也具有抗免疫的作用。此外有研究称其还具有抗疼痛的作用。但是不幸的是,该药物已折戟临床III 期试验。
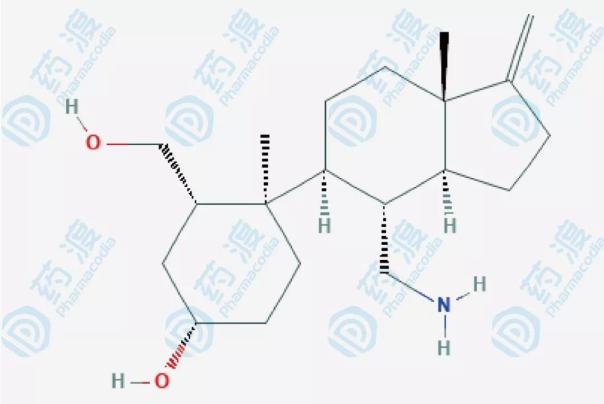
AQX-1125的化学结构
作为“不可成药”靶点的磷酸酶,随着这方面研究的深入,以及临床药物的增加,该靶点及其化合物的作用机制得以一步步解开。目前,该领域中大多数较为成功的药物是基于“变构”理论研发的。有了理论指导,进一步开发相似结构的药物就会简单很多,但也并不是没有挑战。由于磷酸酶带有电荷,与之结合的药物一般具有很强的极性或者也具有电荷,这就导致药物可能具有很差的生物利用度与透膜效果,这极大的影响了药物药效的发挥。如何解决这些难题将是需要面临的现实挑战。

联系我们
服务热线:0755-66853366
市场部:136 7004 6396 (微信同号)
邮箱:sales@chem-strong.com
办公地址:深圳市龙岗区碧新路2055号佳业广场1201室
*本公司所有产品仅供研发使用,不能用于人体或动物临床

联系我们
服务热线:0755-66853366
市场部:136 7004 6396 (微信同号)
邮箱:sales@chem-strong.com
办公地址:深圳市龙岗区碧新路2055号佳业广场1201室
*本公司所有产品仅供研发使用,不能用于人体或动物临床