发布时间:2018-11-06

据药智注册与受理数据,截止目前CDE共承办一致性评价受理号491个,涉及186家企业的184个品种;其中289目录药品受理号有232个,涉及品种69个,289目录药品启动率为23.88%;此外,目前已通过一致性评价受理号达75个(41个品种),其中289目录药品有19个,完成率仅6.57%。
本周(10月25日至11月1日),一致性评价申报新增17个受理号,涉及13家企业的10个品种,劲爆的是其中有9个品种为289目录药品,看来不想放弃的企业仍在加足马力奋力一战;而阿莫西林胶囊企业突然扎堆申报,本周内就有4家企业进行申报,谁将争得第三家获批,我们拭目以待;另外还有1个品种首家申报获受理,为南京先声东元制药的依达拉奉注射液,具体详情一起看看:

(注:由于篇幅有限,图片未完全展示,如有需要的朋友可进入药智网一致性评价进度数据库查看更多详情)
依达拉奉注射液
10月29日,南京先声东元制药的依达拉奉注射液一致性评价获CDE承办。
依达拉奉是一种脑保护剂(自由基清除剂),用于治疗急性脑梗死,改善急性脑梗塞所致的神经症状、日常生活活动能力和功能障碍。由日本三菱东京制药株式会社研制开发,2001年在日本批准上市,2004年先声药业首家在国内上市该药品。
据药智数据,目前我国有依达拉奉注射液国产批文18条,生产企业14家,当前南京先声东元制药首家申报一致性评价获受理,抢得先机。另外,据药智一致性评价进度数据库(企业分析)显示,截止目前,南京先声东元制药申报一致性评价共有两个品种,除了依达拉奉注射液,还有瑞舒伐他汀钙片,而瑞舒伐他汀钙片的1个规格已经通过,另一规格在审评审批当中。
阿莫西林胶囊
本周,阿莫西林一致性评价申报甚是火热,10月25日,浙江亚太药业和昆明贝壳诺顿制药相继获得CDE承办;10月29日,四川制药制剂获承办;10月30日,四川依科制药该品种又获得承办。
据药智数据,阿莫西林胶囊现有国产批文241条,涉及生产企业144家,其中,截止目前参比备案一致性评价的企业有61家,16家企业申报获受理,2家企业已通过,为珠海联邦制药和浙江金华康恩贝生物制药,仅差一家企业三足鼎立之势就将形成,到底谁将抢占末位,赢得政策红利,值得期待。

头孢拉定胶囊
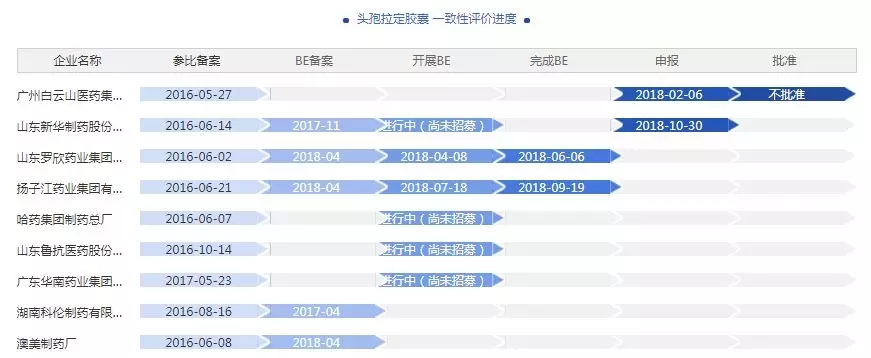
10月30日,山东新华制药头孢拉定胶囊一致性评价获CDE承办。
据药智一致性评价进度数据库,截至目前头孢拉定胶囊一致性评价参比备案的企业有40家,其中申报企业仅广州白云山和山东新华制药2家,值得注意的是广州白云山未能通过,山东新华是否能够抓住机会成为首家通过企业,拭目以待。
头孢呋辛酯片
10月30日,国药集团汕头金石制药头孢呋辛酯片一致性评价获CDE承办。
据药智一致性评价进度数据库,头孢呋辛酯片进行参比备案的企业有12家,其中已有9家企业申报获受理,值得一提的是成都倍特、国药致君、珠海联邦制药已相继通过一致性评价,三足鼎立之势已形成,但是依然不减其他企业申报的热情,毕竟一致性评价关乎企业该品种生死存亡。

甲硝唑片
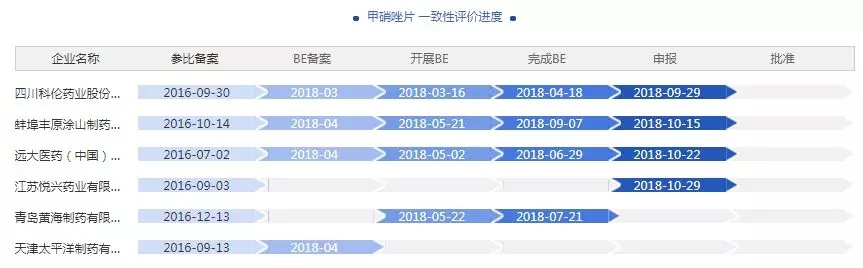
10月29日,江苏悦兴甲硝唑片一致性评价获CDE承办。
据药智一致性评价进度数据显示,甲硝唑片参比备案一致性评价的企业共有55家,申报获受理的企业共有4家,截止目前还没有企业通过,但是四川科伦,蚌埠丰原涂山制药、远大医药皆已完成BE实验,静候佳音。
苯磺酸氨氯地平片
10月29日,宜昌东阳光长江药业苯磺酸氨氯地平片一致性评价获CDE承办。
据药智一致性评价进度数据库,苯磺酸氨氯地平片参比备案的企业有44家,截止目前申报企业达16家,江苏黄河、扬子江、华润赛科药业3家已经通过,但苯磺酸氨氯地平片作为289目录药品的明星药,企业申报持续不断。

富马酸比索洛尔片
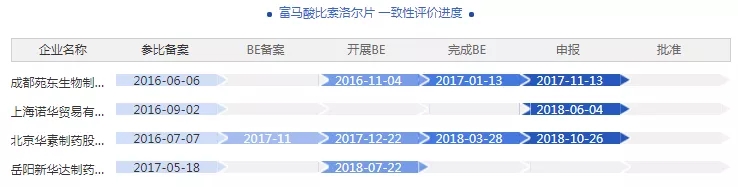
10月26日,北京华素制药富马酸比索洛尔片一致性评价获CDE承办。
据药智一致性评价进度数据库,截止目前富马酸比索洛尔片参比备案的企业有4家,其中3家企业申报,均还未通过。然据进度条显示,成都苑东生物制药虽申报时间最早,但北京华素制药率先完成各环节任务,两家企业谁将首家通过,获取政策福利,一起期待。
盐酸二甲双胍缓释片
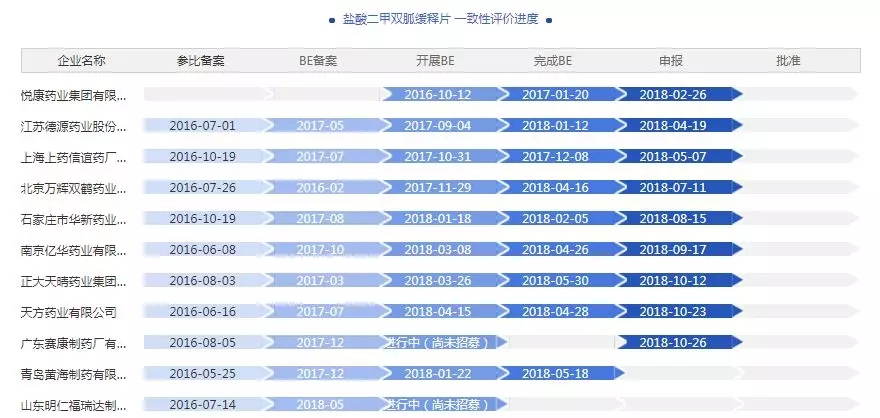
10月26日,广东赛康制药盐酸二甲双胍缓释片一致性评价获CDE承办。
据药智一致性评价进度数据库,现有23家企业参比备案盐酸二甲双胍缓释片一致性评价,申报企业达9家,其中7家企业已完成中间环节工作,均在冲刺首家过一致性评价。更多详情见下表:
依非韦伦片
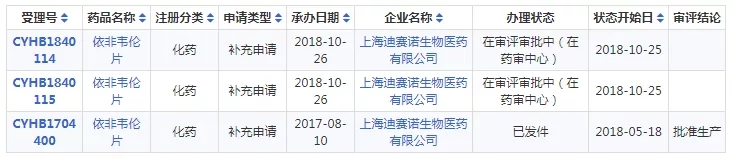
10月25日,上海赛诺生物医药依非韦伦片一致性评价又有两受理号获CDE承办。
据药智数据,目前国内仅华海药业和上海赛诺生物医药2家企业生产依非韦伦片,其中上海赛诺生物医药其中一个受理号已获批生产,详情可见下表:
盐酸二甲双胍片
10月25日,重庆科瑞制药盐酸二甲双胍片一致性评价获CDE承办。
据药智一致性评价数据库,截止目前,盐酸二甲双胍片一致性评价参比备案的企业有51家,申报企业达8家。目前已经有2家企业通过,北京四环制药是按照一致性评价补充申请申报获得通过,而石药欧意的盐酸二甲双胍片则以美国ANDA上市的优势转报国内成功,纳入《中国上市药品目录集》,视同通过一致性评价。目前申报获受理的8家企业也均已完成一致性评价中间环节工作,都在为抢占末位发起最后的冲刺。


联系我们
服务热线:0755-66853366
市场部:136 7004 6396 (微信同号)
邮箱:sales@chem-strong.com
办公地址:深圳市龙岗区碧新路2055号佳业广场1201室
*本公司所有产品仅供研发使用,不能用于人体或动物临床

联系我们
服务热线:0755-66853366
市场部:136 7004 6396 (微信同号)
邮箱:sales@chem-strong.com
办公地址:深圳市龙岗区碧新路2055号佳业广场1201室
*本公司所有产品仅供研发使用,不能用于人体或动物临床